Tacrolimus (면역 억제제)
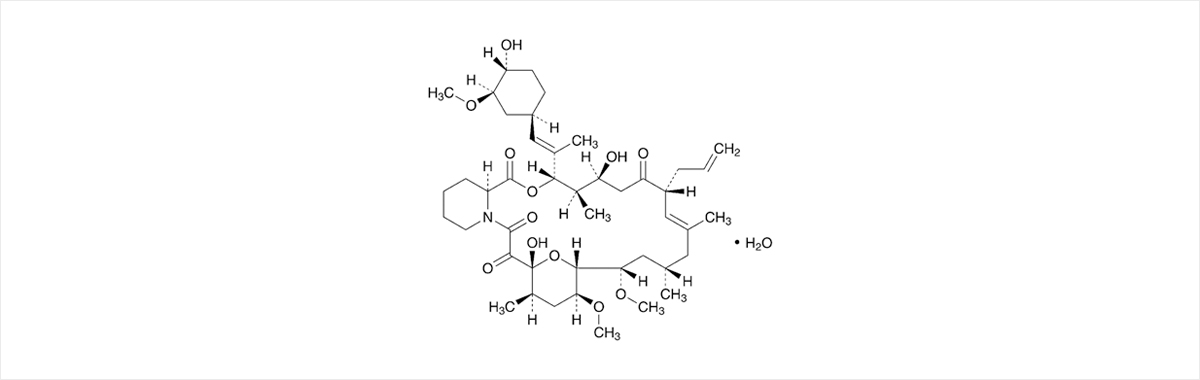
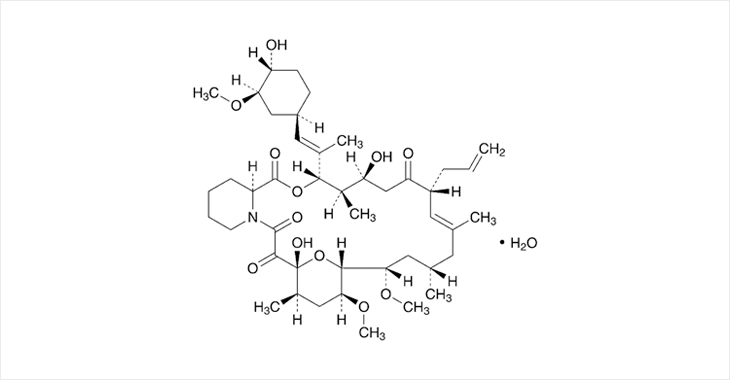
C44H69NO12·H2O
-
타크로리무스(Tacrolimus)는 면역억제 활성 및 항진균 활성을 가지는 마크로라이드 계열의 이차 대 산물이며 장기이식 환자의 면역거부반응을 억제하기 위하여 사용하고 있을 뿐 아니라
아토피와 같은 자가면역질환의 치료에도 사용됩니다. 타크로리무스는 강력하고 잠재력 높은 면역억제제이며, 현재 가장 널리 사용되고 있는 면역억제제인 cyclosporin 보다 10배에서
100배 이상의 면역억제효과를 나타내고 있으며 부작용면에서도 다모증이나 치육증식 혹은 고혈압 등의 증상이 감소된 형태로 나타난다고 알려져 있습니다. -
(주)세레스에프엔디에서는 2003년부터 미생물 생리활성물질의 산업화 기술 개발연구를 수행하여 타크로리무스의 산업적 생산을 위한 고생산 균주 개발 및 발효
(특허 제 2007-0082624 호), 의약품 기준에 적합한 고순도 정제공정 개발 (특허 제 2008-0091523 호 및 제 2008-0091521 호), 타크로리무스의 생합성 관련 유전자의 연구 및 이용
(특허 제 2008-0118854 호)등 우수한 품질관리를 위한 타크로리무스 및 그 유연물질의 분석법 개발을 지속적으로 수행하였으며, 이러한 특허 기술을 토대로 타 크로리무스의 상업적 생산을
위한 lab scale에서 plant scale까지 scale up 연구 등을 통해 2009년 품목 등록을 하여 생산하고 있습니다.
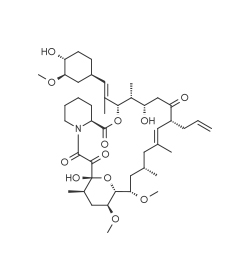
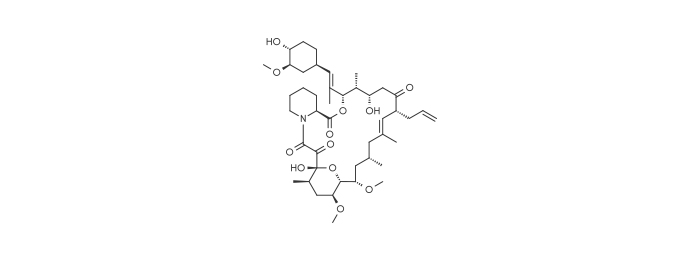
Tacrolimus (FK506)
- 생산 균주 : Streptomyces tsukubaensis
- 구조 : polyketides(Macrolide) ※ 화학 합성 불가
- 성상 : 흰색 비결정성 분말 ※ 수용성 매우 낮음 (water solubility: 4㎍/㎖)
- 특허 : 주요 특허 2008년 만료
- 개발 역사 : 1984년 일본 Fujisawa co. Ltd에서 개발, Astellas에서 PROGRAF®로 발매
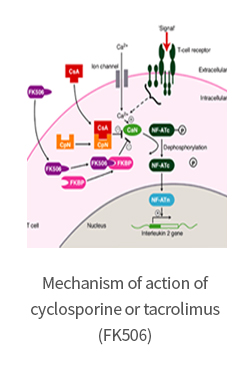
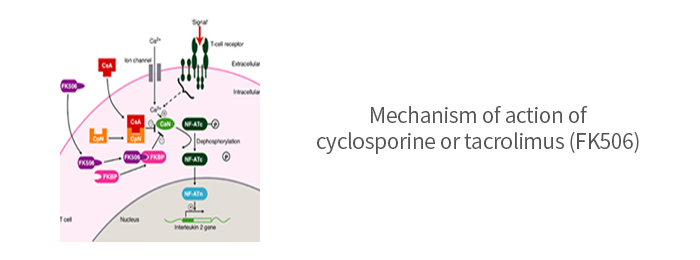
작용기전 (Calcineurin억제제)
타크로리무스는 FKBP-12와 결합하여 칼슘 / Calmodulin 의존성 단백질인, 칼시 뉴린 (calcineurin)의 활성을
억제함으로써, NF-AT의 탈인산화 및 전위를 방지하고 IL-2, TNF-α 및 발암원인 유전자의 전사를 억제한다.
따라서, 타크로리무스는 T- 림프구 활성화에 대한 강력한 억제 효과를 나타낸다.
적응증
- 장기이식 환자 면역치료제
- 난용성 Capsule 형태로 경구 복용
- 이식거부반응의 억제제로 평생에 걸쳐 장기 복용
- 중증 아토피 치료제 (연고제 형태)
당사 보유 Tacrolimus 기술 및 특허
| 특허번호 | 제 목 | 특 징 |
|---|---|---|
| WO2011068341A2 | * 유전공학적 타크로리무스를 포함한 방선균속 삼원환 화합물의 생산, 변형 및 불순물 저감하는 기술 |
유전자 재조합으로 만든 고순도 타크로리무스 생산 가능 |
| US8193345 B2 | ** 은이온 용액 추출을 이용한 불포화 알킬기를 가진 락톤 | 독보적 불순물 정제기술 확보 (정제 수율이 극대화) |
| WO2013022238 | *** 당화 삼원환 화합물 합성을 통한 수용성증가로 만들어지는 개량신약 후보 물질과 적응증의 예 |
물리적 제제화 (에멀젼 등)의 안정성을 극복한 신규화합물 |
- *방선균주의 유전공학적 접근으로, 고순도 타크로리무스 대량 생산이 가능해짐
- **FK520, DH-tacro, FK525등의 불순물의 완벽한 제거와 은이온 재사용으로 생산비용 절감
- ***단당,이당,삼당류 들의 연속적인 화학적 결합으로 수용해성의 1,000배이상 증가로 다양한 제제를 만들고, 추가적인 적응증에 사용할 개량신약 후보물질 소개
CERTIFICATE OF ANALYSIS
Product Name : Tacrolimus Hydrate(IP/JP/USP/Ph.Eur)| Test | Specification | |
|---|---|---|
| Description | A white crystal or white crystalline powder | |
| Solubility | Very soluble in methanol and ethanol, Freely soluble in N,N-dimethylformamide, Soluble in ethyl acetate, Sparingly soluble in hexane, In soluble in water and heptane | |
| Identification | IR | The IR spectrum of sample should be concordant with that of standard |
| HPLC | The retention time of the major peak of the Sample solution corresponds to that of the Standard solution as obtained in the Assay | |
| Color | Red-purple color develops | |
| Optical Rotation | -110 to -115 | |
| Appearance of solution | 1. The solution is clear and not more intensely colored than reference solution GY7 | |
| 2. Dissolve 0.2g in ethanol and dilute to 20 ml with same solvent | ||
| Water content | NMT 4.0% | |
| Residue on ignition | NMT 0.1% | |
| Organic impurities, Procedure 1 | Tacrolimus methylacryl aldehyde | NMT 0.2% |
| Tacrolimus diene | NMT 0.2% | |
| Any individual unspecified impurity | NMT 0.2% | |
| Total impurities | NMT 0.3% | |
| Organic impurities, Procedure 2 | Ascomycin 19-epimer | NMT 0.1% |
| Ascomycin | NMT 0.5% | |
| Desmethyl tacrolimus (if present) | NMT 0.1% | |
| Tacrolimus 8-epimer | NMT 0.15% | |
| Tacrolimus 8-propyl analog | NMT 0.15% | |
| Any individual unspecified impurity | NMT 0.1% | |
| Total impurities | NMT 1.0% | |
| Residual Solvent | Hexane | NMT 290 ppm |
| Acetone | NMT 5,000 ppm | |
| Ethylacetate | NMT 5,000 ppm | |
| Heptane | NMT 5,000 ppm | |
| Assay (by HPLC, on anhydrous and solvent free basis) | 98.0 to 102.0% | |
| Storage: Store protected from moisture and at a controlled temperature below 30℃ | ||
| This is USP version. Specification will be changed for IP/JP/Ph.Eur | ||
